
 2026-02-09
13:36:27
2026-02-09
13:36:27自2024年12月13日欧盟《通用产品安全法规》(简称“GPSR”)正式生效以来,欧盟市场对医疗器械的合规监管进一步升级。
线上销售的医疗器械必须配备合规GPSR欧盟负责人,否则按法规要求对其进行欧盟市场屏蔽及订单拦截。
近期,TEMU、阿里巴巴、亚马逊等线上平台也开始加强合规稽查,已有不少未配备合规GPSR欧盟负责人、或信息虚假、冒用、失效的商家,被强制下架相关商品、或者直接被退仓,无法发货。
1、GPSR欧盟负责人义务
- 保存欧盟GPSR符合性声明,定期检查技术文件、产品信息。
- 产品或包装或随附文件上应显示欧盟负责人的名称、地址、E-mail/URL。
- 配合主管当局上市后监察,纠正产品不合规问题,确保符合欧盟要求。
注:欧盟负责人必须是在欧盟境内设立的制造商、授权代表、进口商、履约服务提供商。
2、线上平台核查
- 线上平台会要求厂商录入欧盟负责人信息、上传协议,并关联适用产品;之后平台人员会进行GPSR合规性审核。
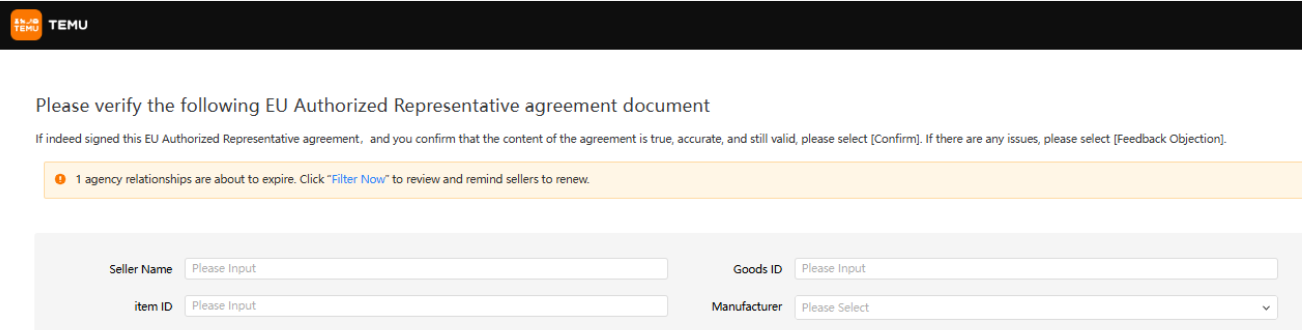
- 部分平台,还会发邮件给欧盟负责人。例如我们经常收到来自TEMU和亚马逊的通知,要求核验厂商上传的欧盟负责人服务协议,判断信息是否真实、有效。
3、厂商应该怎么做?
- 自查现有欧盟负责人合规性:确保合作机构资质齐全、授权合同完整有效。
- 主动排查合规隐患:检查产品包装、线上详情页是否清晰标注欧盟负责人信息。
- 选择专业欧盟负责人:若未配备欧盟负责人,或现有欧盟负责人不合规(比如厂商将自己的欧盟境内子公司作为欧盟负责人但实际上不具备承担上市后风险的能力),需尽快选择正规机构展开合作。
在此呼吁所有相关商家:
线上医疗器械销售的合规要求只会越来越严格,商家需要高度重视GPSR欧盟负责人合规,及时补齐合规短板,切勿因一时疏忽,导致商品下架、罚款、市场受限等不可挽回的损失。
合规不是成本,而是长期发展的底气。
 / 地址:
/ 地址:
 / 电话:
+49251 322 66-64
/ 电话:
+49251 322 66-64  / 电邮:
contact@mednet-ecrep.com
/ 电邮:
contact@mednet-ecrep.com